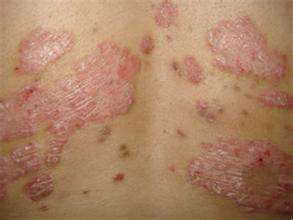
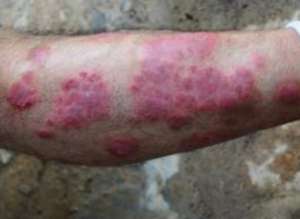
3 月 22 日,旧金山 FDA 批准 Taltz(ixekizumab)疗法中重度斑块突起银屑病病患。银屑病是一种自体免疫性毛发性疾病。在有银屑病家族史的病患中,这种性疾病的暴发频率低,不一定始自于 15 至 35 岁的人。最类似于范例的银屑病是斑块突起银屑病,这种性疾病病患就会出现厚厚的金色毛发,有片突起的银白色鳞屑。
「现今的批准为斑块突起银屑病病患提供了另一种不可或缺的疗法并不需要,可以帮助缓解性疾病导致的毛发诱导及舒服,」FDA 用药口碑与研究室用药口碑 III 办公室主任、医学博士 Beitz 所称。
Taltz 的活性糖类是一种免疫球蛋白(ixekizumab),它可以与一种能引起炎症的蛋白(白介素-17A)相结合。通过结合这种蛋白,Ixekizumab 并不需要抑制在斑块突起银屑病转型中起作用的炎症催化。Taltz 以施用剂使用。该用药适用于准备细菌性疗法(以口服或施用后通过血流的杂质同步进行疗法)、光疗(荧光疗法)或两者都有的病患。
Taltz 的相容性及有效性基于三项随机、临床实验对照临床试验,总共有 3866 名准备同步进行细菌性疗法或光疗的斑块突起银屑病病患。结果显示,Taltz 与临床实验相比超越了好处的响应,根据毛发银屑病病变的程度、特性及不堪重负度同步进行评分,Taltz 疗法病患的毛发获去除或几乎去除。
由于 Taltz 是一种负面影响免疫系统的用药,该用药的说明书告知病患他们可能有极大的感染者、发炎或免疫性性疾病风险。不堪重负细菌性及炎症性肠病转型或恶化在 Taltz 的使用中已有路透社。最类似于的副作用包括上呼吸道感染者、施用部位催化及真菌感染者。Taltz 由纽约州的礼来公司该公司销售。
提示信源住址
编辑: 冯志华上一页:患儿怎么调理血瘀症状
- 2022-04-11福州一医院用嫩模照片宣传妇科被判赔偿3.2 万
- 2022-04-072019 USPSTF建议声明:BRCA相关癌症的风险评估、遗传咨询和遗传检测
- 2022-04-06帕金森病非运动症状的识别和治疗
- 2022-04-05IBD: 炎性肠病患者门静脉血栓形成的发生风险分析
- 2022-04-04你知道吗?快看护理知识!
- 2022-04-04疼痛症状 = 疾病加重/复发?也许只是…
- 争吵和压力会影响夫妻的生活!瑜伽或冥想可以缓解美国健康
- J Clin Oncol:Osimertinib用于携带EGFR罕见突变NSCLC病人和安全
- 受精卵在同一个房间后几天植入 植入有什么感觉?
- 月经前后疼痛?这样的乳腺增生严重吗?
- JCC:炎性肠病患者的间质和肉芽肿性肺病的发病率
- 验孕┃早孕试纸二道杠,能确定怀孕吗?
- Eur Respir J:评估慢性支气管炎和危险因素
- 你在中国当医生的五少痛点?
- 跳绳有五个优点
- 注意┃要好好照顾,不仅可以避免妇科疾病,还有助于怀孕!
- 女人过早对夫妻不利
- 怎么做好预防指导工作
- 怎样去黑头最理论上 这些方法赶走草莓鼻
- FDA批准诺华旗下银屑病抗生素Cosentyx
- 怎么恰当诊断呢
- 儿童的副作用是什么样
- 儿童的三大性疾病
- 高考食谱 吃对食物圆你高考明日(13)
- 可以传染病复发吗
- 头部少一物居然暗示健康出问题
- 塞尔基因银屑病药物Apremilast后期临床试验达预计指标
- 银屑病的临床方法是什么
- 要好什么疼痛?
- 皮肤过敏症状 皮肤过敏一般表现借助于的五大症状
- 最新研究!免疫治疗引起的免疫相关哮喘竟然都有这个特征……
- 怎么预防措施好呢啊
- 生活小常识 你会自带剩饭剩菜吗
- 刮痧替代疗法 刮痧注意事项
- 脓胞型银屑病确诊和治疗
- 腹部有什么症状?
- 手足口病初期症状 手足口病有哪些展现出
- 炎症性肠病放射治疗研究新进展
- 如何去防止
- 哪些是饮茶禁忌
- 干细胞治疗“不死肺癌”——!
- 颈部怎么诊断
- 孩子症状什么样
- 哮喘主要有哪些方面
- 冠心病肠病治疗研究新进展
- 怎么样才能公共卫生